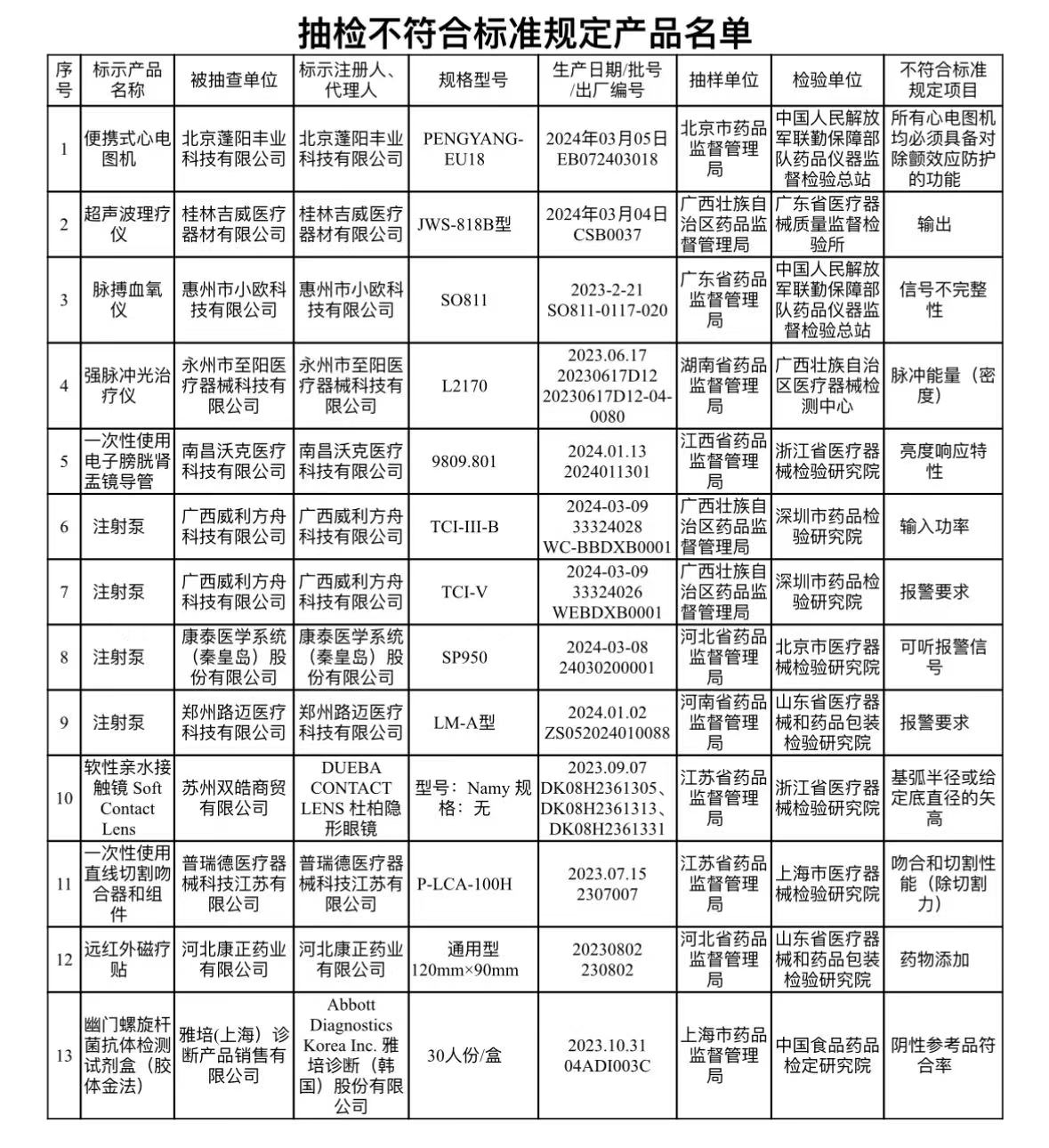
4台注射泵被检出问题。分别为广西威利方舟科技有限公司、康泰医学系统(秦皇岛)股份有限公司、郑州路迈医疗科技有限公司生产,涉及输入功率、报警要求、可听报警信号不符合标准规定。
康泰医学是一家专业从事医疗诊断、监护设备的研发、生产和销售的企业,产品涵盖血氧类、心电类、超声类、监护类、血压类等多个大类。2020年8月24日,在深交所创业板上市,是创业板注册制下第一批上市的18家公司之一。
此外,9批(台)不合规医疗器械信息如下:
心电图机1台:北京蓬阳丰业科技有限公司生产,涉及项目“所有心电图机均必须具备对除颤效应防护的功能”不符合标准规定。超声治疗设备1台:桂林吉威医疗器材有限公司生产,涉及输出不符合标准规定。医用脉搏血氧仪1台:惠州市小欧科技有限公司生产,涉及信号不完整性不符合标准规定。强脉冲光治疗仪1台:永州市至阳医疗器械科技有限公司生产,涉及脉冲能量(密度)不符合标准规定。电子内窥镜1台:南昌沃克医疗科技有限公司生产,涉及亮度响应特性不符合标准规定。
软性接触镜1批:DUEBA CONTACT LENS 杜柏隐形眼镜生产,涉及基弧半径或给定底直径的矢高不符合标准规定。直线型吻(缝)合器1批:普瑞德医疗器械科技江苏有限公司生产,涉及吻合和切割性能(除切割力)不符合标准规定。贴敷类医疗器械1批:河北康正药业有限公司的远红外磁疗贴,涉及检出“按照补充检验方法要求不得检出的相关药物成分”。幽门螺杆菌抗体检测试剂1批:Abbott Diagnostics Korea Inc. 雅培诊断(韩国)股份有限公司生产,涉及阴性参考品符合率不符合标准规定。